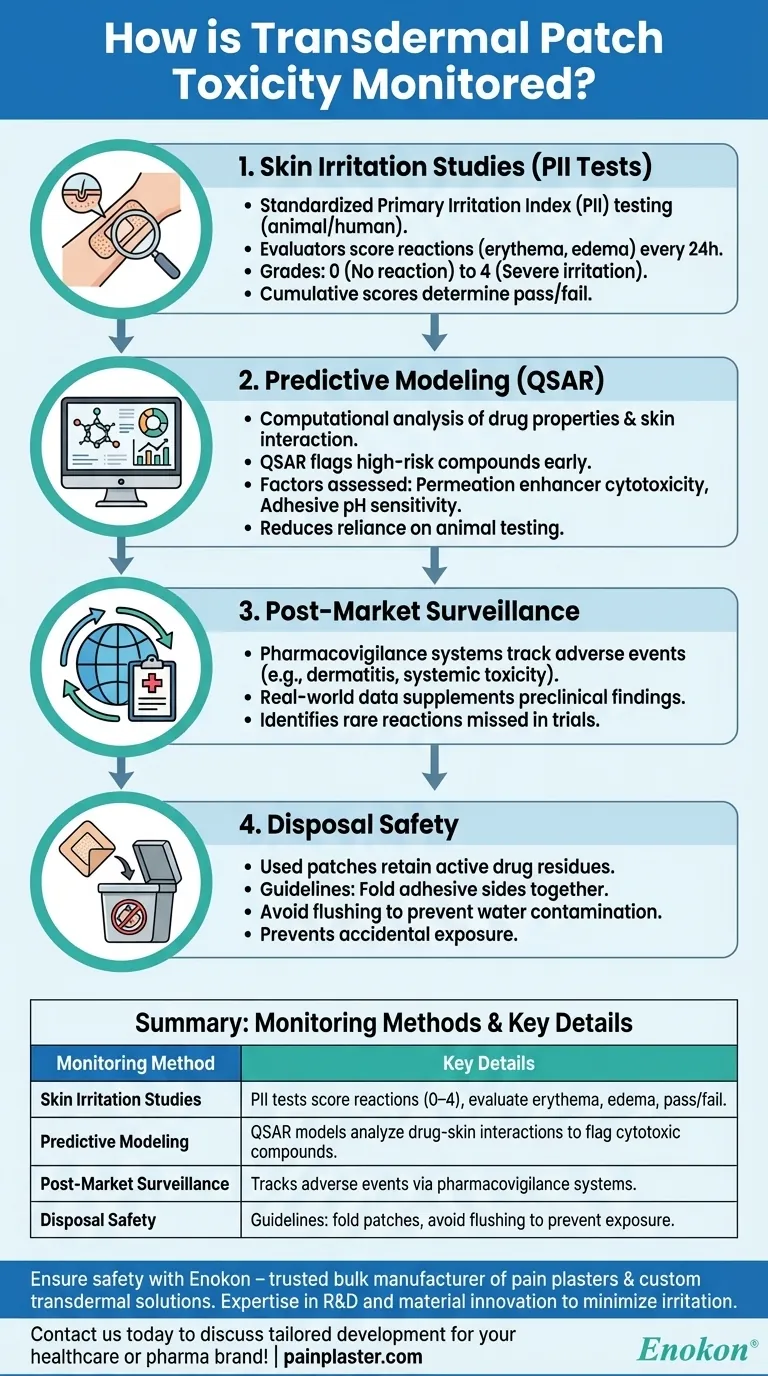
経皮吸収型テープ製剤の毒性は、前臨床の皮膚刺激性試験、予測モデリング、および市販後のサーベイランスを組み合わせてモニタリングされる。主な方法としては、紅斑や浮腫のような局所的な皮膚反応を評価する一次刺激性指数(PII)試験や、薬物と皮膚の相互作用を解析する計算モデルなどがある。二次暴露リスクを防ぐためには、適切な廃棄プロトコールが不可欠である。これらの重層的なアプローチにより、開発から実際の使用までの安全性が確保される。
キーポイントの説明
-
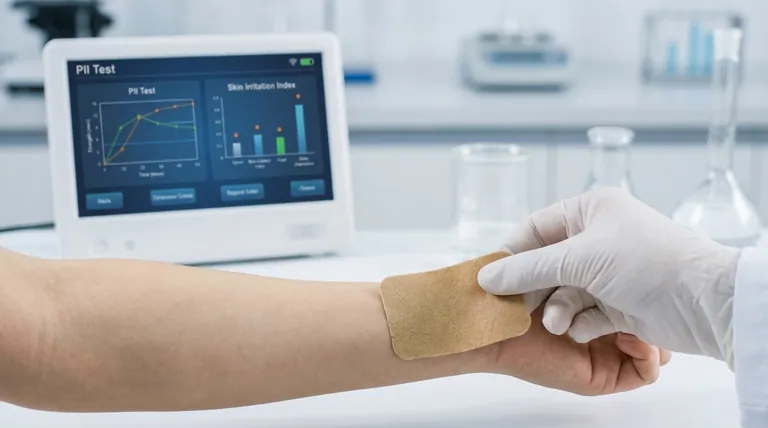
皮膚刺激性試験(PII試験)
- その 経皮パッチ は、標準化された一次刺激性指数(PII)試験を受け、管理された条件下で動物またはヒトの皮膚にパッチが適用される。
-
評価者は24時間間隔で反応(発赤、腫脹)を採点し、グレードをつける:
- 0(反応なし)~4(強い刺激)。
- 累積スコアにより、さらなる開発のための合否基準値が決定される。
-
予測モデリング
- 計算ツールは、薬物の特性(溶解度、分子量など)や皮膚層との相互作用を解析する。
- QSAR(Quantitative Structure-Activity Relationship:定量的構造活性相関)のようなモデルは、リスクの高い化合物に早期にフラグを立て、動物実験への依存を減らす。
-
評価される要因
- 浸透促進剤の細胞毒性。
- 粘着層のpH感受性
-
市販後調査
- ファーマコビジランスシステムは、医療従事者や患者から報告された有害事象(接触性皮膚炎、全身毒性など)を追跡する。
- 実世界のデータは前臨床の知見を補足し、臨床試験で見逃された稀な反応を特定する。
-
廃棄の安全性
- 使用済みパッチには活性薬剤が残留している。不適切な廃棄は、偶発的な曝露(例、小児/ペット)の危険性がある。
-
ガイドラインは以下の通り:
- 廃棄前に粘着面を一緒に折り畳むこと。
- 水の汚染を防ぐため、水洗を避ける。
-
新たな技術
- マイクロニードルアレイと生分解性素材は、薬物送達の精度を高めつつ、刺激リスクを軽減することを目的としている。
これらの戦略を統合することで、メーカーは有効性と患者の安全性のバランスをとり、有害性を最小限に抑えながら、パッチが規制基準を満たしていることを保証します。将来のデザインにおいて、素材の革新がどのように刺激をさらに軽減するかを検討したことがありますか?
総括表
| モニタリング方法 | 主な内容 |
|---|---|
| 皮膚刺激性試験 | PII試験は、紅斑、浮腫、合否の閾値を評価するために反応をスコア化(0~4)する。 |
| 予測モデリング | QSARモデルで薬剤と皮膚の相互作用を解析し、細胞毒性を持つ化合物を早期に発見する。 |
| 市販後調査 | 有害事象(皮膚炎など)をファーマコビジランスシステムで追跡。 |
| 廃棄の安全性 | ガイドラインには、曝露を防ぐためにパッチを折りたたむこと、水洗を避けることが含まれます。 |
経皮吸収パッチを安全基準に適合させるには エノコン -エノコンは、信頼性の高い貼付剤およびカスタム経皮吸収型製剤のバルクメーカーです。当社の研究開発および材料イノベーションの専門知識は、有効性を最大限に高めながら、刺激リスクを最小限に抑えるのに役立ちます。 今すぐお問い合わせください あなたのヘルスケアまたは製薬ブランドのためのカスタマイズされた開発についてご相談ください!
ビジュアルガイド