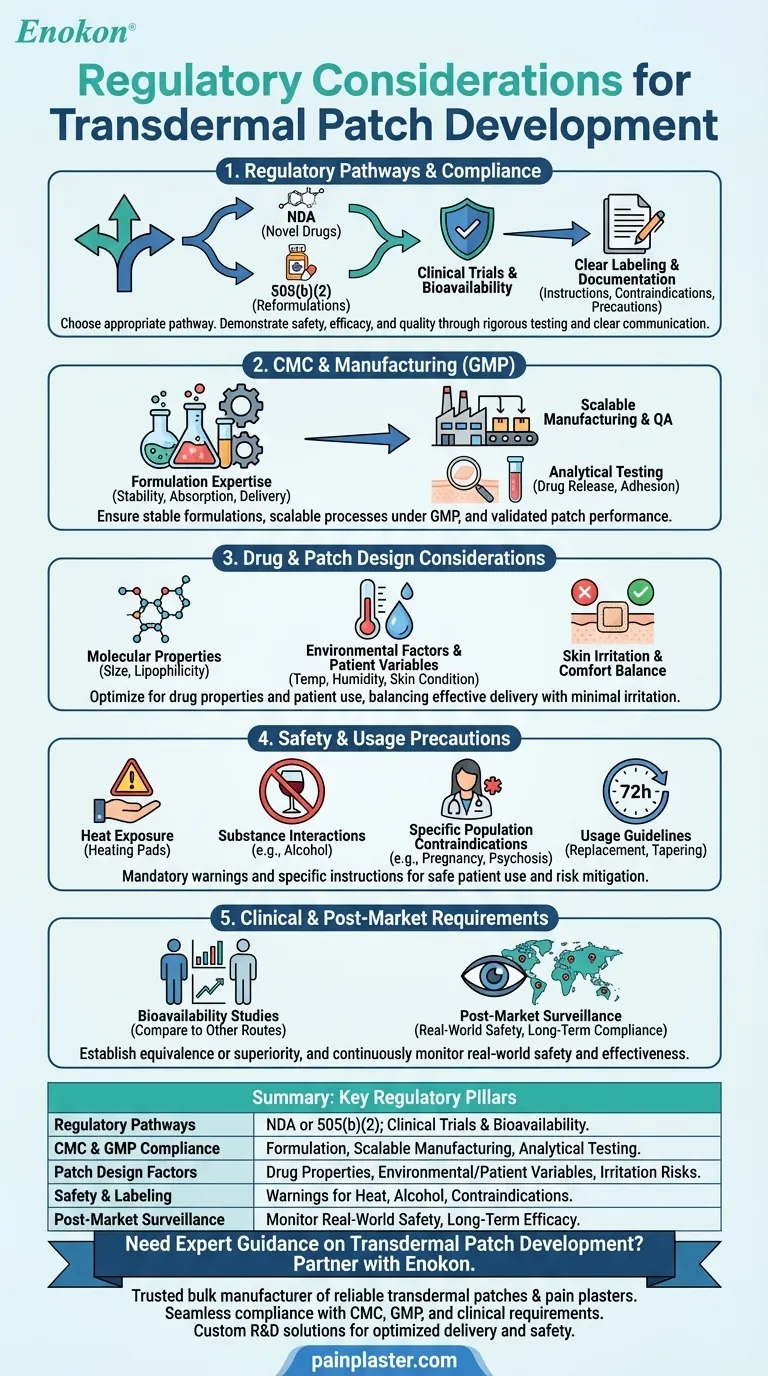
経皮吸収型テープ製剤の開発には、安全性、有効性、および品質を確保するために、複雑な薬事規制を乗り越えることが必要である。主な考慮事項としては、化学・製造・管理(CMC)要件の遵守、適正製造規範(GMP)の順守、バイオアベイラビリティと安全性に関する徹底的な臨床試験などが挙げられる。パッチのデザインは薬物の特性(分子サイズ、極性など)や環境要因を考慮する必要があり、ラベル表示や文書化は厳格な基準を満たす必要がある。医薬品の新規性によっては、NDAや505(b)(2)のような規制経路が適用されることもある。皮膚刺激のリスクや使用上の制限(例えば、熱への曝露を避ける)などの注意事項も、承認を得て患者の安全を確保するために対処しなければならない。

キーポイントの説明
-
規制パスウェイとコンプライアンス
- スポンサーは、新薬のための新薬承認申請(NDA)か、承認済みの医薬品の再製剤のための505(b)(2)経路のどちらかを選択しなければならない。
- コンプライアンス 経皮吸収パッチ の規制では、バイオアベイラビリティ試験を含む臨床試験を通じて、安全性、有効性、品質を実証することが求められている。
- 使用上の注意、禁忌(例:認知症に関連した精神病)、注意事項(例:アルコールや熱への曝露を避ける)を詳細に記載した明確な表示と文書化が義務付けられている。
-
化学・製造・管理(CMC)
- 製剤の専門知識は、薬物の安定性、吸収性、安定した送達速度を確保するために不可欠である。
- 商業生産におけるスケーラビリティと品質保証は、GMP基準に沿ったものでなければならない。
- 分析試験では、薬物放出プロファイルや粘着特性など、パッチの性能を検証する。
-
薬剤とパッチのデザインに関する考察
- 分子特性(例:小さなサイズ、親油性)は吸収率に影響するため、開発中に最適化する必要がある。
- 環境因子(温度、湿度)や患者特有の変数(皮膚の状態、年齢)は有効性に影響するため、現実的な条件下での試験が必要となる。
- パッチは薬物送達と快適さのバランスをとり、皮膚刺激やアレルギー反応を最小限に抑える必要がある。
-
安全性および使用上の注意
- 添付文書には、皮膚刺激、熱曝露(例、温熱パッド)、アルコールなどの物質との相互作用などのリスクに対する警告が必要である。
- 特定の集団(妊娠中/授乳中の人、精神病患者)には禁忌が必要な場合がある。
- 使用ガイドライン(例:72時間ごとの交換、漸減プロトコール)を患者に明確に伝えなければならない。
-
臨床及び市販後要件
- バイオアベイラビリティ試験は、経皮投与と他の経路(経口投与など)を比較し、同等性または優越性を立証する。
- 市販後調査は現実の安全性を監視し、長期的なコンプライアンスを確保し、予期せぬ副作用に対処する。
これらの分野に取り組むことで、開発者は効果的で患者に優しい経皮療法を提供しながら、規制上のハードルを乗り越えることができる。薬物送達を損なうことなく皮膚刺激を軽減するために、パッチ用粘着剤をどのように進化させるか、検討したことがありますか?
要約表
| 主な規制上の考慮事項 | 詳細 |
|---|---|
| 規制経路 | 新薬のNDA、再製剤の505(b)(2)。臨床試験とバイオアベイラビリティ試験が必要。 |
| CMCおよびGMPコンプライアンス | 製剤安定性、スケーラブルな製造、分析試験(薬物放出、粘着性)。 |
| パッチデザイン要因 | 薬物特性(サイズ、親油性)、環境/患者変数、皮膚刺激リスクを最適化する。 |
| 安全性および表示 | 熱曝露、アルコールとの相互作用、高リスク集団に対する禁忌について警告する。 |
| 市販後調査 | 承認後の実際の安全性と長期的な有効性を監視します。 |
経皮吸収型テープ製剤の開発で専門家の指導が必要ですか? パートナー エノコン エノコン社は、ヘルスケアブランドや流通業者向けに、信頼性の高い経皮吸収型テープ製剤と貼付剤を提供するバルクメーカーです。当社の技術的専門知識は、CMC、GMP、および臨床試験要件へのシームレスなコンプライアンスを保証し、当社のカスタムR&Dソリューションは薬物送達と患者の安全性を最適化します。 お問い合わせ までご連絡ください!
ビジュアルガイド
関連製品
- 遠赤外線鎮痛パッチ 経皮吸収パッチ
- シリコンスカーシートパッチ 経皮吸収型薬剤パッチ
- アイシーホット・メンソール薬用痛み止めパッチ
- メントール・ジェル・ペイン・リリーフ・パッチ
- よもぎの痛み止めパッチ(首の痛み用